178亿!国产创新药勇夺第一
来源:
欧宝全站app
发布时间:2024-04-24 22:11:04
属于国家管控危险化学品,根据相关法规和网安部门规定,本网站不提供该产品相关销售信息。
在其发布的2024年Q1业绩预增公告中,营收6亿元至6.2亿元,同比增长82.12%至88.21%,再次实现单季由亏转盈。
不仅如此,根据此前公布的2023年报,其核心产品重组八因子安佳因销售额约17.8亿元,同比增幅超过77%,占据同种类型的产品市场占有率第一。
安佳因在获批之前,国内已有5款进口重组凝血因子VⅢ药品,分别为拜耳的拜科奇和科跃奇、百特的百因止、辉瑞的任捷,以及诺和诺德的诺易,且就其获批后一个月,又迎来另一款进口产品(韩国绿十字株式会社的绿茵芷)在国内获批入局。
据药智多个方面数据显示,2020年,国内重组凝血因子VⅢ的销售额为11.68亿元,但市场基本被拜耳、百特和辉瑞把持,分别占市场占有率的53.68%(6.27亿元)、27.65%(3.23亿元)和14.73%(1.72亿元)。
安佳因是神州细胞的首 款获批上市产品,在2021年7月获国家药监局批准用来医治成人及青少年(12岁)血友病A患者出血的控制和预防,成为第一个获批上市的国产重组人凝血因子VⅢ产品。
面对进口药“前有强敌,后有追兵”的竞争格局,神州细胞的安佳因异军突起,在上市后第一个完全年度销售额达10.23亿元,据神州细胞2023年报显示,安佳因销售额继续大幅度增长,约为17.8亿元,同比增长超77%,已实现同种类型的产品市场占有率第一,预计2024年有望破20亿元大关。
正在向国际市场进军。神州细胞在开发安佳因的战略上,国际市场一开始就在其布局中,包括了成人预防治疗和儿童预防治疗两项临床研究,由于2020年IPO募集资金不足,并未执行,但在2021年又向特定对象发行股票募集资金且获证监会同意。
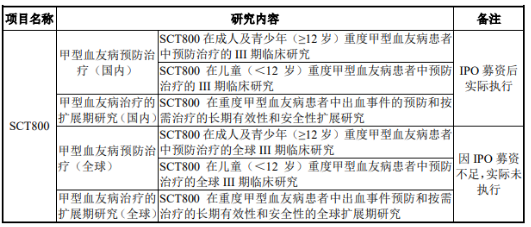
2023年1月,随着安佳因用于12岁以下儿童甲型血友病患者的新增适应症获批,神州细胞对安佳因在国内的开发基本结束,转战国际市场正在慢慢地推进中。
值得一提的是,神州细胞针对重组八因子工艺过程中出现的杂质,开发出专用的亲和层析介质,大幅度提高纯度和纯化收率,实现了高效产业化,一条生产线亿国际单位(IU),接近全球数十厂家产量总和,且比活达7590-13340IU/mg蛋白,高于国内外同种类型的产品比活标准。
截至目前,神州细胞已与印度、土耳其、印尼、斯里兰卡、巴西、巴基斯坦等合作伙伴签约,利用合作方在当地的临床、注册和销售经验,推动安佳因在当地商业化,且在2023年已分别向巴基斯坦、巴西、印度尼西亚和印度提交了注册申请。
神州细胞第一个产品安佳因在2022年为其带来10.23亿元的营收,但同时也让神州细胞的营收成为典型的单一产品结构,据2022年报显示,其全年总营收全部来自安佳因。
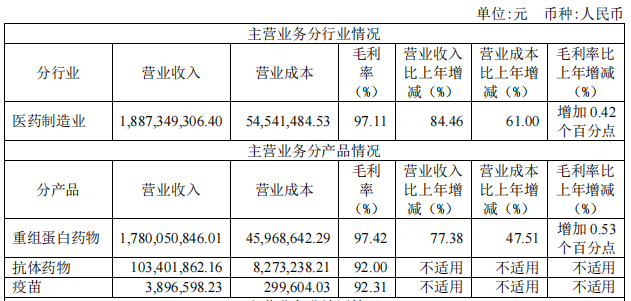
一年“不见”,产品矩阵初具规模。随着安平希、安佳润和安贝珠等3款产品的获批上市,2023年,神州细胞已实现盈利收入从单一产品向多产品的华丽转身,据2023年报显示,除了安佳因在重组蛋白药物领域实现了17.8亿元的营收外,其他3款产品合计在抗体药领域实现盈利收入1.03亿元,不计新冠疫苗的营收,神州细胞产品2023年营收合计为18.83亿元,安佳因和其他3款产品分别占比为94.51%和5.49%。
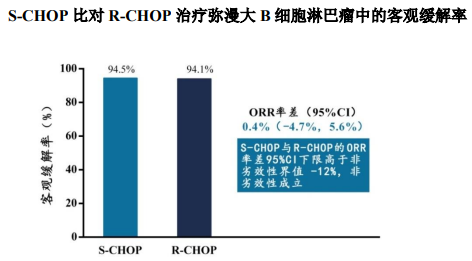
安平希是神州细胞获批上市的第一个抗体药物,也是第一个抗肿瘤产品,虽是参照利妥昔单抗(美罗华)研发的人鼠嵌合抗CD20单抗新药,但一级结构与美罗华不完全相同,并非生物类似药,在某些临床数据上甚至略优于原研药。
据3期头对头临床试验结果为,安平希(S-CHOP组:237人)和美罗华(R-CHOP组:118人)治疗弥漫大B细胞淋巴瘤患者的客观缓解率分别为94.5%和94.1%,此外,在总生存率上,安平希和美罗华分别为91.5%和90.1%。尽管两组间差异无统计学显著性意义,但非劣效性,让安平希在患者选择非生物类似药的情况下,有了替代原研药的实力,在2023年12月,成功进入国家医保目录。
另外2款产品中,安佳润为阿达木单抗生物类似药,安贝珠为贝伐珠单抗生物类似药,均在2023年6月获批,值得一提的是,神州细胞在开发2款生物类似药上下足了功夫,均是一次性获批原研药当时在国内获批的全部适应症,虽然在当年获批时间较晚,但均在2023年实现销售收入。
创新药临床管线双突破。神州细胞在创新药管线上的产品较多,据招股书显示多达21款,但截至2020年5月,只有SCT1000、SCT800(安佳因)、SCT400(安平希)、SCT200、SCTI10A和ASCT510A等6款产品进入临床阶段。
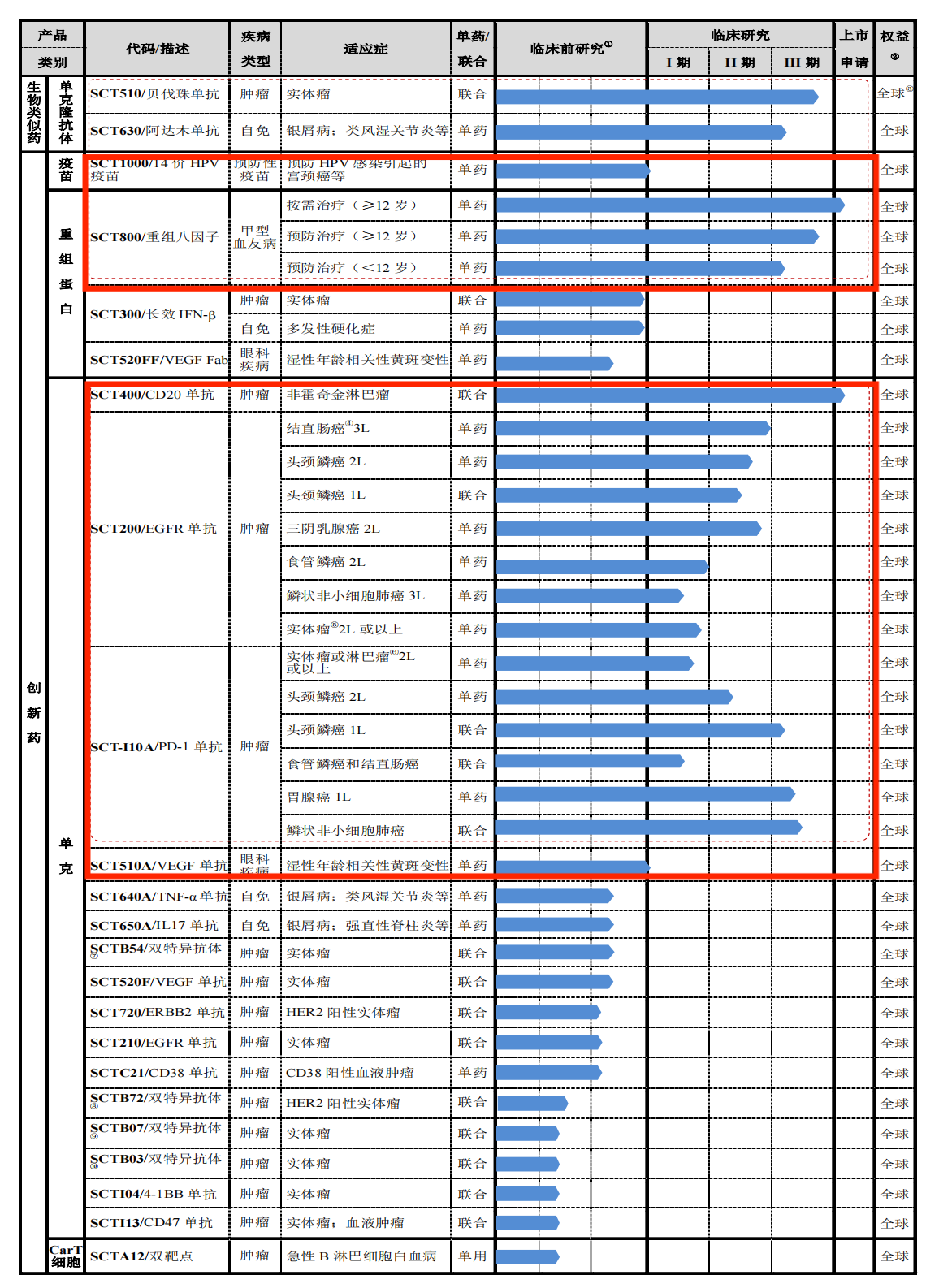
到2023年12月,神州细胞创新药产品管线上,除了因新冠而新增的创新药产品进入临床外,也仅只有自主研发的IL-17单抗SCT650C,在澳大利亚被推进至临床阶段。
随着安佳因在市场上的持续火爆,以及别的产品获批上市后对营收的助力,神州细胞有了加快创新药临床进程的底气,2024年1月以来,已有3款新药获批临床,分别为SCTC21C、SCTB35和SCTB14,值得一提的是,3款产品均为自主研发,其中SCTB35和SCTB14为双特异性抗体药。
卧薪尝胆多年的神州细胞,在创新药管线产品临床进展上终于迎来数量和种类的双突破。
据神州细胞2023年报显示,在研产品中处于3期临床及以上的有2款,分别为上市申请获受理的SCTI10A和处于3期临床的SCT1000,其中,前者为PD-1单抗,后者为HPV疫苗,受PD-1/L1赛道的拥挤影响,即便是临近获批的SCTI10A,也挡不住还未NDA的SCT1000。
HPV市场再生变。国产2价HPV疫苗的获批,已让国内甚至全球HPV疫苗市场有过一次从进口产品手中夺回市场的剧变,万泰生物的2价馨可宁,作为国产首 款HPV疫苗,曾一度风光无限,2022年批签发量超2800万剂,沃森生物的2价沃泽惠,在2022年3月获批上市,当年也有498万剂的批签发量。
然而,随着葛兰素史克2价HPV疫苗9-14岁女性两剂次接种程序的获批,以及默沙东9价HPV疫苗年龄的扩展,特别是接种者追求“高价疫苗高保护”的消费观念下,国产2价疫苗打响的价格战又一次引发市场关注,据资料显示,2024年3月,馨可宁在江苏的中标价为86元/支,相比之前中标价(329元/支),降幅达73.86%。
SCT1000是全球第一个进入临床的14价HPV疫苗,基于9价疫苗增加5个新价型(HPV35、39、51、56、59型),覆盖世界卫生组织评估的12个高危致癌HPV病毒型和2个最主要导致尖锐湿疣HPV病毒型。
尽管还有一款国产15价HPV疫苗,是目前获IND批准最高价次疫苗,但在2024年3月才启动1期临床试验,因此,SCT1000成为最有潜在实力收割进口9价疫苗市场的选手,且对其他绝大多数国产HPV疫苗也能形成威胁。
曾靠多次募集资金推动临床进展的神州细胞,随着自我造血功能的逐渐增强,脚下的创新路也将越走越宽。
最高支持额度50亿,多省市出台支持医药创新政策;中国生物制药引进多款管线
神州细胞启动14价HPV疫苗III期临床;先博生物CD19 NK细胞疗法临床获批
K药大卖250亿美元锁定新“药王”,HPV疫苗营收89亿美元 默沙东2023年财报
2024年首例生物科学技术IPO诞生;沃森生物去年净利润下降37%-45%
更多
Blenrep是GSK开发的一款靶向B细胞成熟抗原的ADC药物。由于DREAMM-3研...[详细]
近日,吉利德科学(Gilead Sciences)和一家临床阶段生物技术公司X...[详细]
今年前三个月只有10种新药取得授权(表1)。按照最近的标准,2...[详细]
美国FDA授予辉大基因的迷你型dCas13X-RNA碱基编辑器疗法儿科罕见病...[详细]
肠道菌群是肠道微生态系统的重要组成部分,人类在长期进化过程...[详细]